Химик РУДН вместе с коллегами из Институтов РАН упростили синтез противоопухолевых соединений
и Института биологии развития им. Н.К. Кольцова РАН разработали новый метод синтеза производных изоксазола — веществ, которые дестабилизируют процесс деления клеток и в перспективе могут стать основой для новых противораковых препаратов. Новый способ основан на использовании легкодоступных реагентов и не требует высоких температур.
Многие современные противоопухолевые препараты токсичны, труднодоступны и/или очень дороги. Кроме того, опухолевые клетки могут развивать устойчивость к применяемым препаратам. Поэтому исследователи изучают биологические свойства молекул, чтобы получить новые противоопухолевые препараты с оптимальными свойствами. Один из распространённых подходов к поиску таких препаратов - тестирование аналогов веществ с уже доказанной противоопухолевой активностью. В число таких веществ входят, в частности, производные изоксазола, которые ингибируют — «выключают» — белок Hsp90, необходимый для выживания опухолевых клеток. Однако соединения этого класса малодоступны из-за сложности процедуры синтеза, которая требует, в частности, полного отсутствия молекул воды, а реагенты дороги и токсичны.
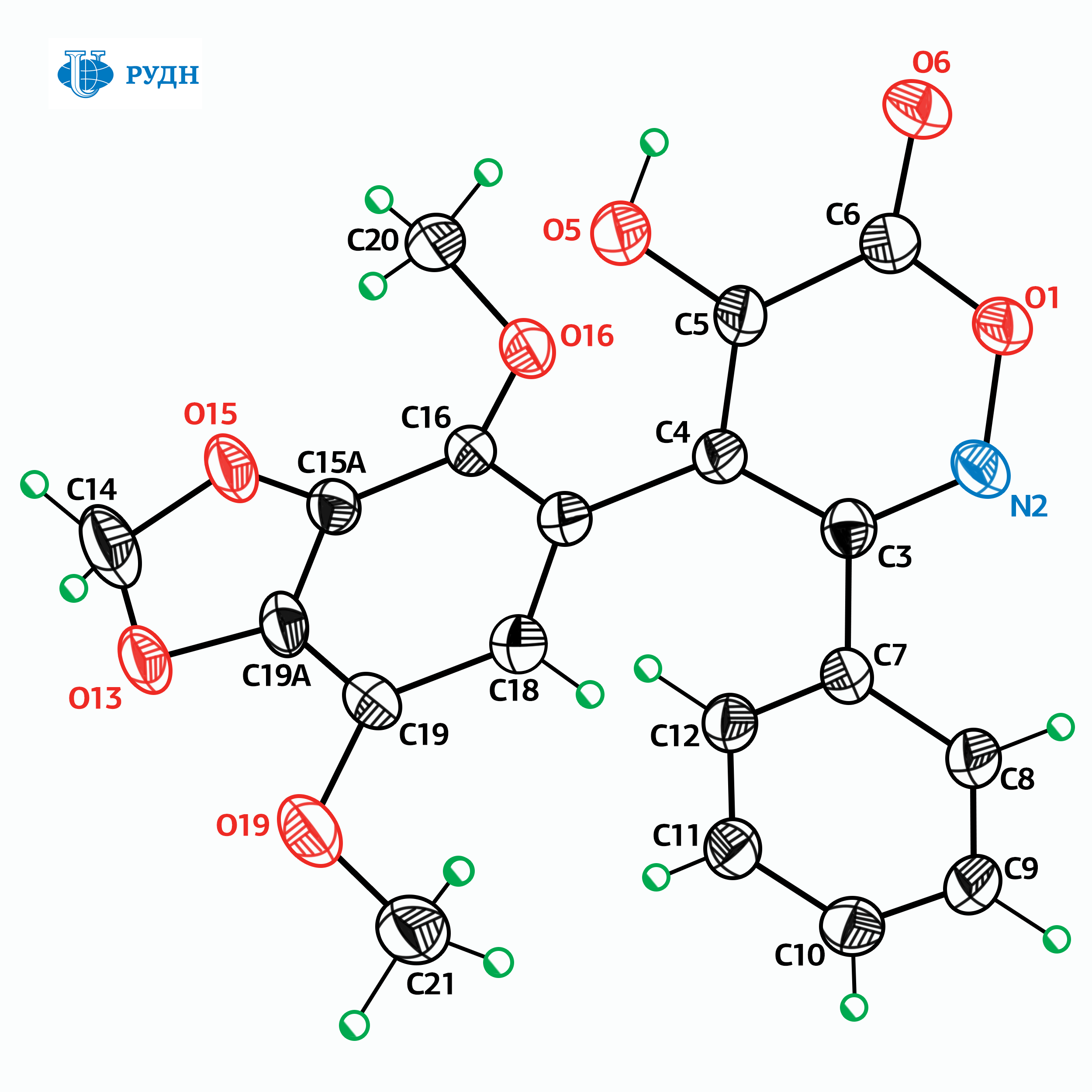
Химик из РУДН Виктор Хрусталев и его коллеги разработали метод синтеза изомеров этих веществ, то есть соединений, одинаковых по атомному составу, но различающихся по расположению атомов в пространстве. В качестве сырья использовали легкодоступные производные арилнитрометанов и хлороацетамидов, а сама реакция шла при температурах не более 80 градусов при атмосферном давлении и не требовала безводных условий.
У полученных веществ была зафиксирована противораковая активность, но в отличие от соединений-прототипов,
они не ингибируют белок Hsp90. Механизм их действия основан на дестабилизации процесса деления
клетки – они препятствуют образованию микротрубочек, которые необходимы в процессе деления клетки.
Таким же механизмом действия обладают производные таксола - одним из наиболее часто применяемых противоопухолевых средств. На основе полученных учеными соединений может быть создана замена дорогостоящим, малодоступным и высокотоксичным производным таксола в терапии онкологических заболеваний.
Статья в журнале European Journal of Organic Chemistry.
Авторский коллектив высшей школы управления РУДН представил монографию «Цифровой реинжиниринг бизнес-процессов в туристической отрасли России: теория, анализ и разработка инновационных решений».
Даниил Матюнин, студент 3 курса кафедры механики и процессов управления инженерной академии РУДН, стал участником масштабного международного события — научно-технического форума SciTech Forum, объединившего учёных из России, Индии, Китая, Бразилии, ЮАР и Малайзии. Программа форума была посвящена актуальным проблемам освоения внеземного пространства и эксплуатации космических систем.
Продолжаем делиться историями фронтовиков, которые после войны участвовали в создании Университета дружбы народов и воспитывали новое поколение студентов.
Игорь Васильевич Черемискин